Скачать ГОСТ Р 56701-2015 Лекарственные средства для медицинского применения. Руководство по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средствДата актуализации: 01.01.2018
|
| Обозначение: |  ГОСТ Р 56701-2015 ГОСТ Р 56701-2015 |
| Обозначение англ: |  GOST R 56701-2015 GOST R 56701-2015 |
| Статус: | введен впервые |
| Название рус.: | Лекарственные средства для медицинского применения. Руководство по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств |
| Название англ.: | Medicines for medical applications. Guidance on nonclinical safety studies for the conduct of human clinical trials and marketing authorization for pharmaceuticals |
| Дата добавления в базу: | 01.02.2017 |
| Дата актуализации: | 01.01.2018 |
| Дата введения: | 01.07.2016 |
| Область применения: | Стандарт устанавливает рекомендации по планированию доклинических исследований безопасности с целью последующего проведения клинических исследований и регистрации лекарственных средств. Стандарт применим во всех случаях разработки лекарственных препаратов и представляет собой общие положения по их разработке. |
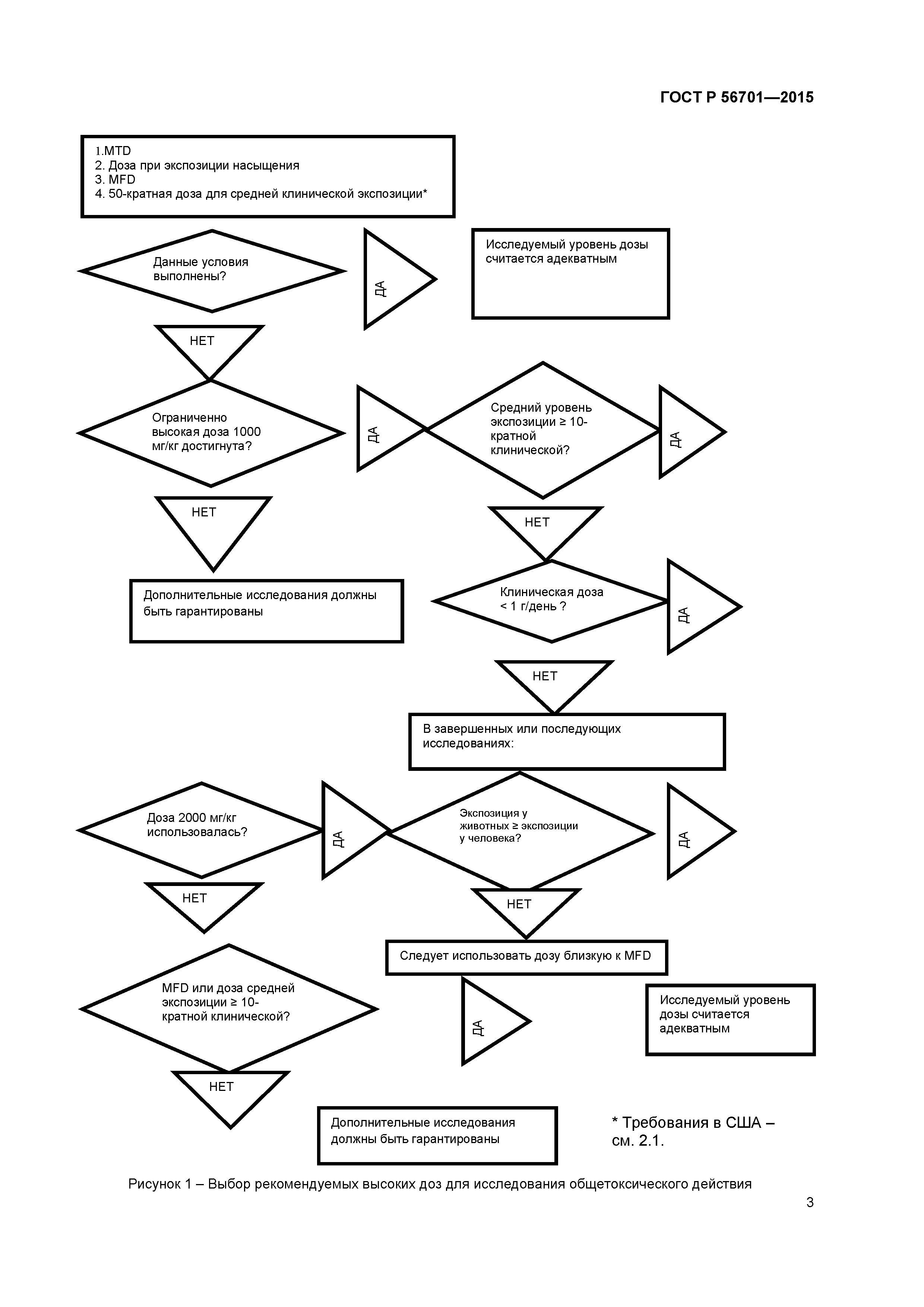
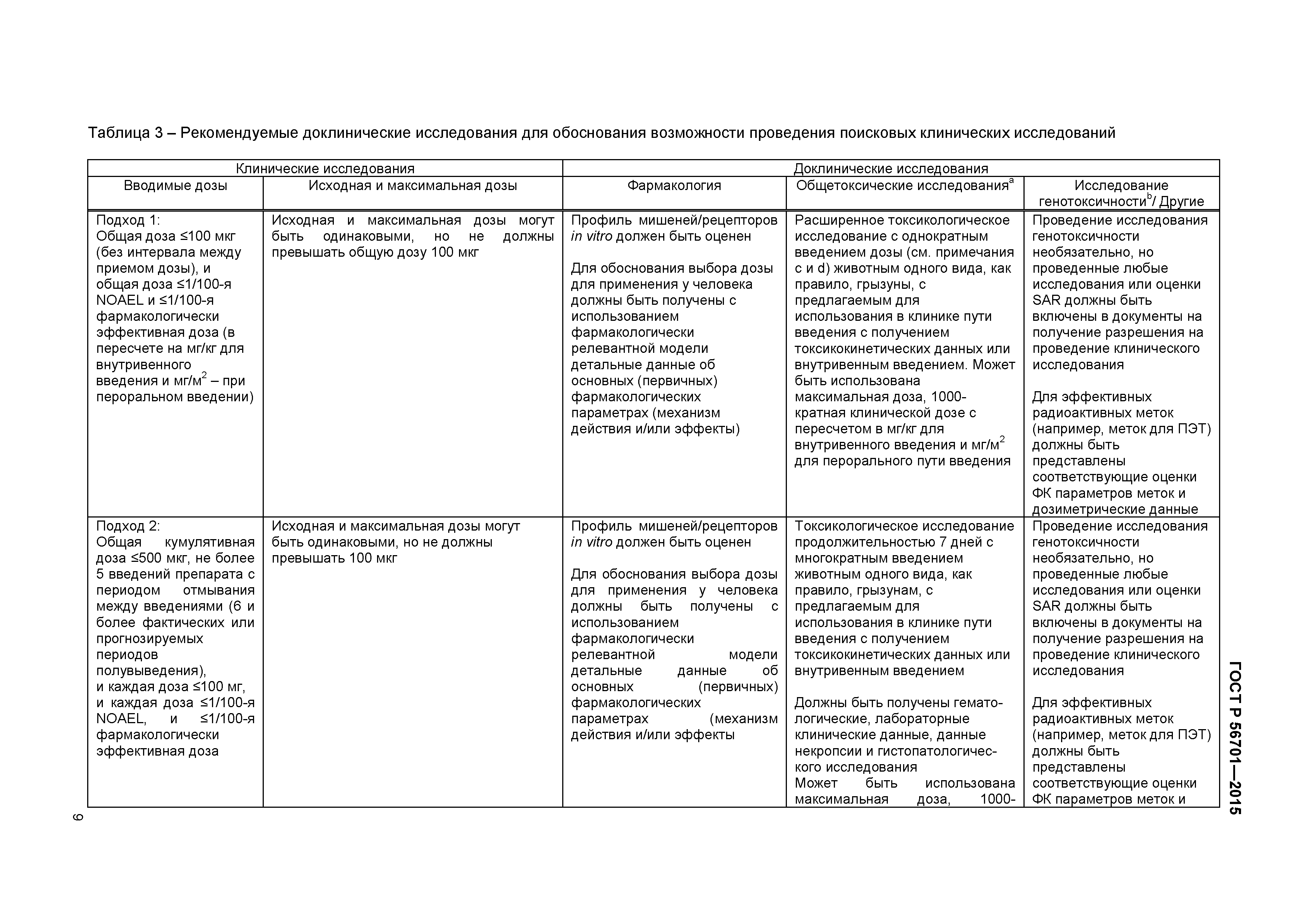
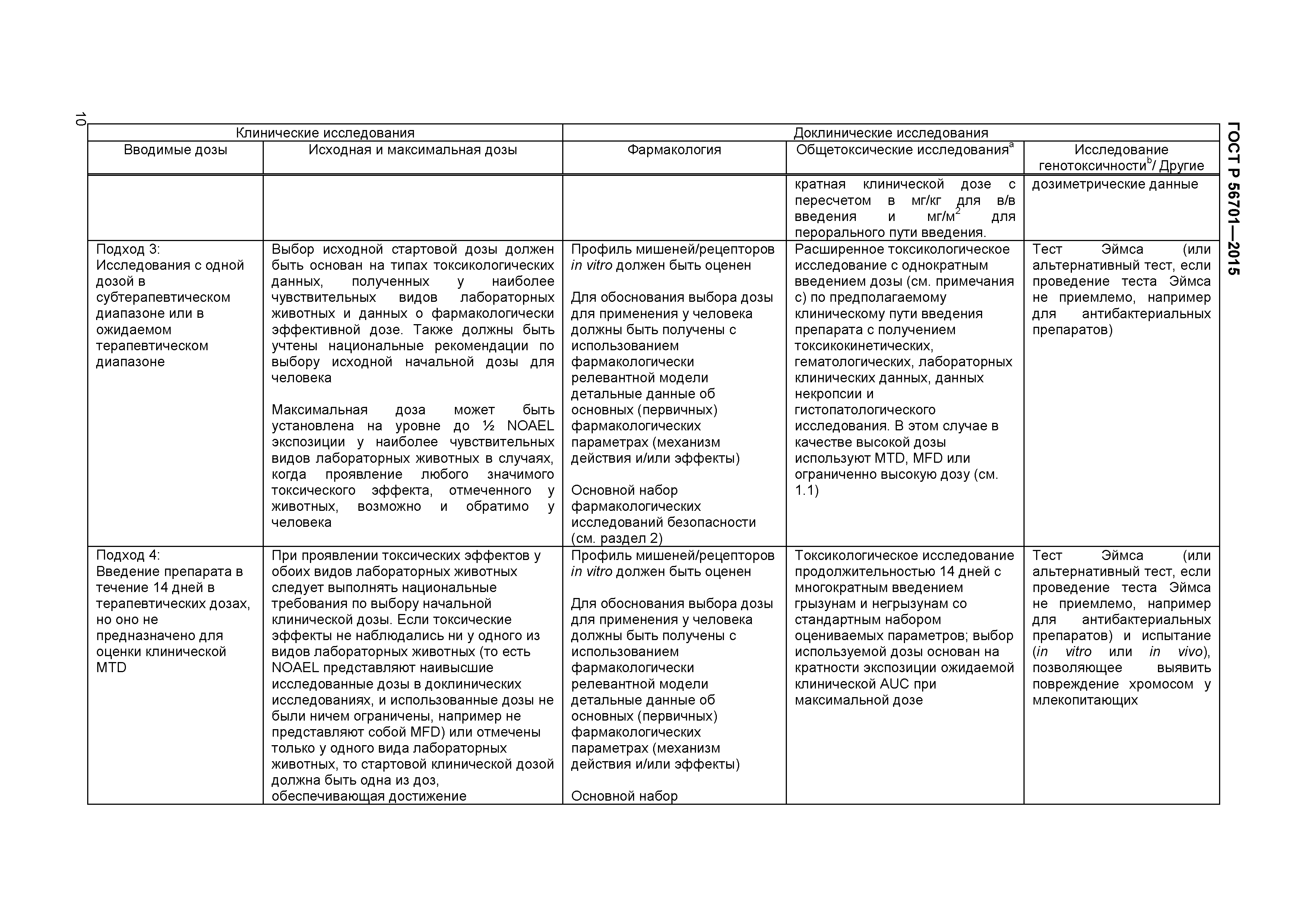
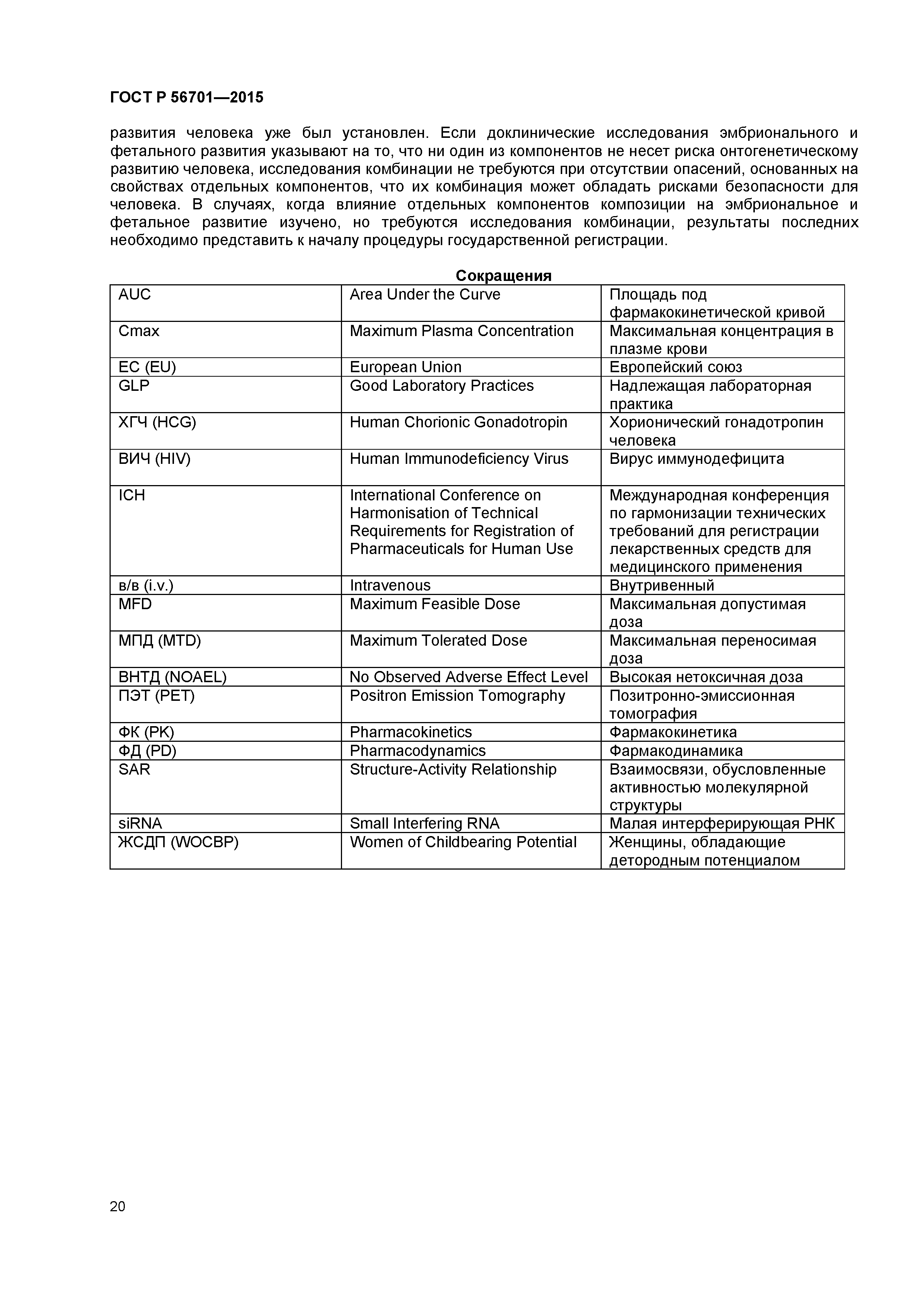
| Оглавление: | 1 Область применения 2 Общие принципы 3 Фармакологические исследования 4 Токсикокинентические и фармакокинетические исследования 5 Исследования острой токсичности 6 Исследования токсичности с многократным введением 7 Определение величины первой дозы у человека 8 Поисковые клинические исследования 9 Исследования местной переносимости 10 Исследования генотоксичности 11 Исследования канцерогенности 12 Исследования репродуктивной токсичности 13 Клинические исследования у педиатрических пациентов 14 Исследование иммунотоксичности 15 Исследование фотобезопасности 16 Доклиническая оценка риска развития лекарственной зависимости 17 Прочие исследования токсичности 18 Изучение токсичности комбинированных лекарственных препаратов Библиография Приложение ДА (справочное) Сведения о соответствии ссылочных международных документов национальным стандартам Российской Федерации |
| Разработан: | ТК 458 Разработка, производство и контроль качества лекарственных средств |
| Утверждён: | 11.11.2015 Федеральное агентство по техническому регулированию и метрологии (1762-ст) |
| Издан: | Стандартинформ (2016 г. ) |
| Нормативные ссылки: |
|
























 ГОСТ Р 53434-2009 «Принципы надлежащей лабораторной практики»
ГОСТ Р 53434-2009 «Принципы надлежащей лабораторной практики»